Kriptón
 From Wikipedia (Es) - Reading time: 13 min
From Wikipedia (Es) - Reading time: 13 min
| Bromo ← Kriptón → Rubidio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tabla completa • Tabla ampliada | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Tubo de descarga lleno de kriptón | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Información general | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nombre, símbolo, número | Kriptón, Kr, 36 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Serie química | Gases nobles | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo, período, bloque | 18, 4, p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masa atómica | 83,80 u | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuración electrónica | [Ar] 3d10 4s2 4p6[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electrones por nivel | 2, 8, 18, 8 (imagen) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apariencia | Incoloro. Exhibe un brillo blanquecino cuando se coloca en un campo eléctrico. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades atómicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Electronegatividad | 3,00 (escala de Pauling) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio atómico (calc) | 88 pm (radio de Bohr) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio covalente | 110 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Radio de van der Waals | 202 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado(s) de oxidación | 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.ª energía de ionización | 1350,8 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.ª energía de ionización | 2350,4 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3.ª energía de ionización | 3565 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4.ª energía de ionización | 5070 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 5.ª energía de ionización | 6240 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 6.ª energía de ionización | 7570 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 7.ª energía de ionización | 10710 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 8.ª energía de ionización | 12138 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Líneas espectrales |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propiedades físicas | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estado ordinario | Gas (no-magnético) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Densidad | (273 K) 3,75 kg/m3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de fusión | 115,79 K (−157 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Punto de ebullición | 119,93 K (−153 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de vaporización | 9,029 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entalpía de fusión | 1,638 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Presión de vapor | _ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varios | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Estructura cristalina | Cúbica centrada en las caras | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Calor específico | 248 J/(kg·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductividad térmica | 0,00949 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidad del sonido | 1120 m/s a 293,15 K (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isótopos más estables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Artículo principal: Isótopos del kriptón | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Valores en el SI y condiciones normales de presión y temperatura, salvo que se indique lo contrario. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
El kriptón o criptón[2] es un elemento químico de la tabla periódica cuyo símbolo es Kr y su número atómico es 36.[3][4] Es un gas noble incoloro, inodoro e insípido que se encuentra en cantidades mínimas en la atmósfera y este a menudo se utiliza con otros gases raros en lámparas fluorescentes. Con raras excepciones, el criptón es químicamente inerte.
El criptón, al igual que los demás gases nobles, se utiliza en iluminación y fotografía . La luz de criptón tiene muchas líneas espectrales, y el plasma de criptón es útil en láseres de gas brillantes y de alta potencia como los láseres de iones de criptón y excimer, cada uno de los cuales resuena y amplifica una sola línea espectral. El fluoruro de criptón también constituye un útil láser medio. De 1960 a 1983, la definición oficial de metro se basó en la longitud de onda de una línea espectral de criptón-86, debido a la alta potencia y la relativa facilidad de operación de los tubos de descarga de criptón.
Características principales
[editar]
El kriptón es un gas noble inodoro e insípido de poca reactividad caracterizado por un espectro de líneas verde y rojo-naranja muy brillantes. Es uno de los productos de la fisión nuclear del uranio. El kriptón sólido es blanco, de estructura cristalina cúbica centrada en las caras al igual que el resto de gases nobles, excepto el helio, que tiene una estructura cristalina compacta hexagonal.
Para propósitos prácticos puede considerarse un gas inerte aunque se conocen compuestos formados con el flúor; además puede formar clatratos con el agua al quedar sus átomos atrapados en la red de moléculas de agua. También se han sintetizado clatratos con hidroquinona y fenol. Es el primero de los gases nobles en orden del período para el que se ha definido un valor de electronegatividad.
El kriptón está presente en el aire aproximadamente en 1 ppm en la atmósfera, lo que representa el 0,0001% de la atmósfera.
Su configuración electrónica termina en 4s2 3d10 4p6
Químicas
[editar]
Como los demás gases nobles, el kriptón es químicamente muy poco reactivo. La química bastante restringida del kriptón en el estado de oxidación +2 es paralela a la del elemento vecino bromo en el estado de oxidación +1; debido a la contracción escándida es difícil oxidar los elementos 4p a sus estados de oxidación de grupo. Hasta la década de 1960 no se habían sintetizado compuestos de gases nobles.[6]
Tras la primera síntesis exitosa de compuestos de xenón en 1962, la síntesis del difluoruro de criptón (KrF
2) se comunicó en 1963. En el mismo año, Grosse, et al. informó de la síntesis de KrF
4[7] pero posteriormente se demostró que era una identificación errónea.[8]
En condiciones extremas, el criptón reacciona con el flúor para formar KrF2 según la siguiente ecuación:
- Kr + F2 → KrF2
El gas criptón en un láser de fluoruro de kriptón absorbe energía de una fuente, haciendo que el criptón reaccione con el gas flúor, produciendo el exciplex fluoruro de criptón, un complejo temporal en un estado energético excitado:
- 2 Kr + F
2 → 2 KrF
El complejo puede sufrir una emisión espontánea o estimulada, reduciendo su estado energético a un estado metaestable, pero altamente repulsivo. El complejo en estado básico se disocia rápidamente en átomos no unidos:
- 2 KrF → 2 Kr + F
2
El resultado es un láser de excímeros que irradia energía a 248 nm, cerca de la porción ultravioleta del espectro, correspondiente a la diferencia de energía entre el estado básico y el estado excitado del complejo.
También se han descubierto compuestos con criptón unido a átomos distintos del flúor. También hay informes no verificados de un bario sal de un oxoácido de criptón.[9] ArKr+ y KrH+ Se han investigado iones poliatómicos y hay pruebas de que KrXe o KrXe+.[10]
La reacción de KrF
2 con B(OTeF
5)
3 produce un compuesto inestable,Kr(OTeF
5)
2 que contiene un enlace criptón- oxígeno . Se encuentra un enlace criptón- nitrógeno en el catión [HC≡N–Kr–F]+
, producido por la reacción de KrF
2 con [HC≡NH]+
[AsF−
6] por debajo de -50 °C.[11][12][6] Se informó que HKrCN y HKrC≡CH (krypton hydride-cyanide y hydrokryptoacetylene) son estables hasta 40 K .[5]
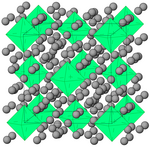
Los cristales de hidruro de criptón (Kr(H2)4) pueden crecer a presiones superiores a 5 GPa. Tienen una estructura cúbica centrada en las caras donde los octaedros de criptón están rodeados por moléculas de hidrógeno orientadas al azar.[5]
Aparición natural
[editar]La Tierra ha retenido todos los gases nobles que estaban presentes en su formación excepto el helio . La concentración de kriptón en la atmósfera es de aproximadamente 1 ppm. Se puede extraer del aire líquido por destilación fraccionada.[13] La cantidad de criptón en el espacio es incierta, porque la medición se deriva de la actividad meteórica y los vientos solares. Las primeras mediciones sugieren una abundancia de criptón en el espacio.[14]
Historia
[editar]
Su nombre proviene del adjetivo griego κρυπτός kryptos cuyo significado es oculto. Fue descubierto en 1898 por los químicos británicos Sir William Ramsay y Morris W. Travers. Ramsay y Travers licuaron aire y lo sometieron a un proceso de destilación fraccionada. Encontraron el kriptón en el residuo dejado por dicho aire líquido justo por encima de su punto de ebullición.
En 1960 la Conferencia General de Pesos y Medidas definió el metro como 1650 763,73 longitudes de onda de luz emitida en el vacío correspondiente a la transición entre los niveles 2p10 y 5d5 del isótopo kriptón-86.[15][16] Debido a errores detectados en el perfil de la línea espectral del kriptón, esta definición del metro se abandonó en 1983. Esto también dejó obsoleta la definición de Ángstrom de 1927 basada en la línea espectral roja de cadmio,[17] reemplazándola con 1 Å = 10−10 m. La definición de kriptón-86 duró hasta la conferencia de octubre de 1983, que redefinió el metro como la distancia que recorre la luz en el vacío durante 1/299 792 458 s.[18][19][20]
Isótopos
[editar]El kriptón natural está constituido por seis isótopos estables y se han caracterizado diecisiete isótopos radiactivos.
El isótopo Kr-81 es producto de reacciones atmosféricas con los otros isótopos naturales, es radiactivo y tiene un periodo de semidesintegración de 250 000 años. Al igual que el xenón, el kriptón es extremadamente volátil y escapa con facilidad de las aguas superficiales por lo que se ha usado para datar antiguas aguas subterráneas (50 000 a 800 000 años).
El isótopo Kr-85 es un gas inerte radiactivo con un periodo de semidesintegración de 10,76 años que se produce en la fisión del uranio y del plutonio. Las fuentes de este isótopo son las pruebas nucleares (bombas), los reactores nucleares y el reprocesado de las barras de combustible de los reactores. Se ha detectado un fuerte gradiente de este isótopo entre los hemisferios norte y sur, siendo las concentraciones detectadas en el polo norte un 30 % más altas que en el polo Sur.
Aplicaciones
[editar]
El kriptón se puede utilizar de diversas formas. La que posee mayor riesgo para la salud es si se lo usa en anestesia, ya que si no se aplica apropiadamente puede causar daños fatales.
Las múltiples líneas de emisión de kriptón hacen que las descargas de gas de Kriptón ionizado parezcan blanquecinas, lo que a su vez hace que las bombillas basadas en kriptón sean útiles en fotografía como fuente de luz blanca. El Kriptón se utiliza en algunos flashes fotográficos para fotografía de alta velocidad. El gas kriptón también se combina con mercurio para hacer señales luminosas que brillan con una luz azul verdosa brillante.[21]
El kriptón se mezcla con argón en lámparas fluorescentes de bajo consumo, lo que reduce el consumo de energía, pero también reduce la salida de luz y aumenta el costo.[22] El criptón cuesta unas 100 veces más que el argón. El kriptón (junto con el xenón) también se usa para llenar lámparas incandescentes para reducir la evaporación del filamento y permitir temperaturas de funcionamiento más altas.[23] Una luz más brillante resulta con más color azul que las lámparas incandescentes convencionales.
La descarga blanca de Kriptón se usa a veces como un efecto artístico en los tubos de "neón" de descarga de gas. El kriptón produce una potencia de luz mucho mayor que el neón en la región de la línea espectral roja y, por esta razón, los láseres rojos para espectáculos de luces láser de alta potencia suelen ser láseres de kriptón con espejos que seleccionan la línea espectral roja para la amplificación y emisión del láser, en lugar de la variedad de helio-neón más familiar, que no podía lograr las mismas salidas de varios vatios.[24]
El láser de fluoruro de kriptón es importante en la investigación de energía de fusión nuclear en experimentos de confinamiento. El láser tiene una alta uniformidad de haz, una longitud de onda corta y el tamaño del punto se puede variar para rastrear una bolita que implosiona.[25]
En la física de partículas experimental, el kriptón líquido se utiliza para construir calorímetros electromagnéticos casi homogéneos . Un ejemplo notable es el calorímetro del experimento NA48 en el CERN que contiene alrededor de 27 toneladas de kriptón líquido. Este uso es raro, ya que el argón líquido es menos costoso. La ventaja del kriptón es un radio de Molière más pequeño de 4,7 cm, que proporciona una excelente resolución espacial con poca superposición.
Los conjuntos de chispas selladas en los excitadores de encendido de algunos motores a reacción antiguos contienen una pequeña cantidad de kriptón-85 para producir niveles de ionización consistentes y un funcionamiento uniforme.
El kriptón-83 tiene aplicación en las imágenes por resonancia magnética (IRM) para obtener imágenes de las vías respiratorias. En particular, permite al radiólogo distinguir entre las superficies hidrofóbicas e hidrofílicas que contienen una vía aérea.[26]
Aunque el xenón tiene potencial para su uso en la tomografía computarizada (TC) para evaluar la ventilación regional, sus propiedades anestésicas limitan su fracción en el gas de respiración al 35%. Una mezcla respiratoria de 30% de xenón y 30% de kriptón es comparable en eficacia para la TC a una fracción de xenón del 40%, a la vez que evita los efectos no deseados de una alta presión parcial del gas xenón.[27]
El isótopo metaestable kriptón-81m se utiliza en medicina nuclear para exploraciones de ventilación/perfusión pulmonar, donde se inhala y se obtienen imágenes con una cámara gamma.[28]
El kriptón-85 en la atmósfera se ha utilizado para detectar instalaciones clandestinas de reprocesamiento de combustible nuclear en Corea del Norte[29] y Pakistán.[30] Estas instalaciones se detectaron a principios de la década de 2000 y se cree que producían plutonio apto para armas.
El kriptón se utiliza ocasionalmente como gas aislante entre los cristales de las ventanas.[31]
El SpaceX Starlink utiliza kriptón como propulsor para su sistema de propulsión eléctrica.[32]
Precauciones
[editar]El criptón se considera un gas no tóxico asfixiante.[33] El criptón tiene una potencia narcótica siete veces superior a la del aire, y respirar una atmósfera con un 50% de kriptón y un 50% de aire natural (como podría ocurrir en caso de una fuga) provoca en los humanos una narcosis similar a la de respirar aire a cuatro veces la presión atmosférica. Esto es comparable al buceo a una profundidad de 30 m (98,4 pies). (ver Narcosis de nitrógeno) y podría afectar a cualquiera que lo respirara. Al mismo tiempo, esa mezcla contendría sólo un 10% de oxígeno (en lugar del 20% normal) y la hipoxia sería una preocupación mayor.
Referencias
[editar]- ↑ [1] Química inorgánica en google libros
- ↑ «Nombres y símbolos en español acordados por la RAC, la RAE, la RSEQ y la Fundéu». 1 de marzo de 2017. Archivado desde el original el 5 de julio de 2017. Consultado el 4 de abril de 2017.
- ↑ Garritz, Andoni (1998). Química. Pearson Educación. p. 856. ISBN 978-9-68444-318-1.
- ↑ Parry, Robert W. (1973). Química: fundamentos experimentales. Reverte. p. 703. ISBN 978-8-42917-466-3.
- ↑ a b c d Kleppe, Annette K.; Amboage, Mónica; Jephcoat, Andrew P. (2014). «New high-pressure van der Waals compound Kr(H2)4 discovered in the krypton-hydrogen binary system». Scientific Reports 4: 4989. Bibcode:2014NatSR...4E4989K. doi:10.1038/srep04989.
- ↑ a b Bartlett, Neil (2003). «The Noble Gases». Chemical & Engineering News. Consultado el 2 de julio de 2006.
- ↑ Grosse, A. V.; Kirshenbaum, A. D.; Streng, A. G.; Streng, L. V. (1963). «Krypton Tetrafluoride: Preparation and Some Properties». Science 139 (3559): 1047-1048. Bibcode:1963Sci...139.1047G. PMID 17812982. doi:10.1126/science.139.3559.1047.
- ↑ Prusakov, V. N.; Sokolov, V. B. (1971). «Krypton difluoride». Soviet Atomic Energy 31 (3): 990-999. S2CID 189775335. doi:10.1007/BF01375764.
- ↑ Streng, A.; Grosse, A. (1964). «Acid of Krypton and Its Barium Salt». Science 143 (3603): 242-243. Bibcode:1964Sci...143..242S. PMID 17753149. S2CID 11607538. doi:10.1126/science.143.3603.242.
- ↑ «Periodic Table of the Elements». Los Alamos National Laboratory's Chemistry Division. pp. 100-101. Archivado desde el original el 25 de noviembre de 2006. Consultado el 5 de abril de 2007.
- ↑ Holloway, John H.; Hope, Eric G. (1998). Sykes, A. G., ed. Advances in Inorganic Chemistry. Academic Press. p. 57. ISBN 978-0-12-023646-6.
- ↑ Lewars, Errol G. (2008). Modeling Marvels: Computational Anticipation of Novel Molecules. Springer. p. 68. ISBN 978-1-4020-6972-7.
- ↑ «How Products are Made: Krypton». Consultado el 2 de julio de 2006.
- ↑ Cardelli, Jason A.; Meyer, David M. (1996). «The Abundance of Interstellar Krypton». The Astrophysical Journal Letters 477 (1): L57-L60. Bibcode:1997ApJ...477L..57C. doi:10.1086/310513.
- ↑ «The BIPM and the evolution of the definition of the metre». Bureau International des Poids et Mesures. 26 de julio de 2014. Consultado el 23 de junio de 2016.
- ↑ Penzes, William B. (8 de enero de 2009). «Time Line for the Definition of the Meter». National Institute of Standards and Technology. Archivado desde el original el 12 de agosto de 2016. Consultado el 23 de junio de 2016.
- ↑ Burdun, G. D. (1958). «On the new determination of the meter». Measurement Techniques 1 (3): 259-264. S2CID 121450003. doi:10.1007/BF00974680.
- ↑ Kimothi, Shri Krishna (2002). The uncertainty of measurements: physical and chemical metrology: impact and analysis. American Society for Quality. p. 122. ISBN 978-0-87389-535-4.
- ↑ Gibbs, Philip (1997). «How is the speed of light measured?». Department of Mathematics, University of California. Archivado desde el original el 21 de agosto de 2015. Consultado el 19 de marzo de 2007.
- ↑ Unit of length (meter), NIST
- ↑ «Mercury in Lighting». Cape Cod Cooperative Extension. Archivado desde el original el 29 de septiembre de 2007. Consultado el 20 de marzo de 2007.
- ↑ Lighting: Full-Size Fluorescent Lamps. McGraw-Hill Companies, Inc. (2002)
- ↑ Properties, Applications and Uses of the "Rare Gases" Neon, Krypton and Xenon. Uigi.com. Retrieved on 2015-11-30.
- ↑ «Laser Devices, Laser Shows and Effect». Archivado desde el original el 21 de febrero de 2007. Consultado el 5 de abril de 2007.
- ↑ Sethian, J.; M. Friedman; M. Myers. «Krypton Fluoride Laser Development for Inertial Fusion Energy». Plasma Physics Division, Naval Research Laboratory. pp. 1-8. Archivado desde el original el 29 de septiembre de 2011. Consultado el 20 de marzo de 2007.
- ↑ Pavlovskaya, GE; Cleveland, ZI; Stupic, KF; Basaraba, RJ et al. (2005). «Hyperpolarized krypton-83 as a contrast agent for magnetic resonance imaging». Proceedings of the National Academy of Sciences of the United States of America 102 (51): 18275-9. Bibcode:2005PNAS..10218275P. PMC 1317982. PMID 16344474. doi:10.1073/pnas.0509419102.
- ↑ Chon, D; Beck, KC; Simon, BA; Shikata, H et al. (2007). «Effect of low-xenon and krypton supplementation on signal/noise of regional CT-based ventilation measurements». Journal of Applied Physiology 102 (4): 1535-44. PMID 17122371. doi:10.1152/japplphysiol.01235.2005.
- ↑ Bajc, M.; Neilly, J. B.; Miniati, M.; Schuemichen, C.; Meignan, M.; Jonson, B. (27 de junio de 2009). «EANM guidelines for ventilation/perfusion scintigraphy». European Journal of Nuclear Medicine and Molecular Imaging 36 (8): 1356-1370. PMID 19562336. doi:10.1007/s00259-009-1170-5.
- ↑ Sanger, David E.; Shanker, Thom (20 de julio de 2003). «N. Korea may be hiding new nuclear site». Oakland Tribune. Archivado desde el original el 9 de abril de 2016. Consultado el 1 de mayo de 2015 – via Highbeam Research.
- ↑ Bradley, Ed; Martin, David (16 de marzo de 2000). «U.S. Intelligence Find Evidence of Pakistan Producing Nuclear Weapons, CBS». CBS Evening News with Dan Rather. Archivado desde el original el 18 de octubre de 2016. Consultado el 1 de mayo de 2015 – via Highbeam Research.
- ↑ Ayre, James (28 de abril de 2018). «Insulated Windows 101 — Double Glazing, Triple Glazing, Thermal Performance, & Potential Problems». cleantechnica.com. Consultado el 17 de mayo de 2018.
- ↑ SpaceX. «Starlink Mission». Escena en 7:10. Archivado desde el original el 14 de enero de 2022. Consultado el 14 de enero de 2022.
- ↑ Propiedades del criptón Archivado el 19 de febrero de 2009 en Wayback Machine.. Pt.chemicalstore.com. Recuperado en 2015-11-30.
Bibliografía
[editar]- William P. Kirk "Krypton 85: a Review of the Literature and an Analysis of Radiation Hazards", Environmental Protection Agency, Office of Research and Monitoring, Washington (1972)
Enlaces externos
[editar] Wikimedia Commons alberga una galería multimedia sobre Kriptón.
Wikimedia Commons alberga una galería multimedia sobre Kriptón.- WebElements.com - Krypton
- EnvironmentalChemistry.com - Krypton
- Krypton at The Periodic Table of Videos (University of Nottingham)
- Krypton Fluoride Lasers, Plasma Physics Division Naval Research Laboratory
 KSF
KSF